新型CAR-T將蝎毒添加到解決腫瘤異質性中,可有效對抗腫瘤
該發現對CAR-T細胞免疫療法領域具有重要意義,它介紹了一種潛在的“通用”CAR治療膠質母細胞瘤的開發和實施。

圖丨該論文發表于《科學轉化醫學》上
CAR-T細胞療法已被批準用于某些形式的白血病和淋巴瘤,并且在治療膠質母細胞瘤的臨床試驗中顯示出一定的抗腫瘤活性,但患者的應答率仍然令人沮喪地低。
膠質母細胞瘤由于腫瘤的異質性而對CAR療法提出了特殊的挑戰:腦癌細胞具有明顯的表型差異,并且并非所有人都攜帶給定CAR-T細胞靶向的特異性抗原,這意味著某些惡性細胞可以逃避攻擊。本文通訊作者Christine Brown解釋說:“我們希望開發一種免疫療法,以識別最大頻率的腫瘤以及這些腫瘤中最大比例的細胞。”
因此,他們向論文一作Dongrui Wang提出挑戰,希望其生成一種包含氯毒素并識別腦癌細胞的CAR。Wang成功了,他的發現促成了該論文的成功發表。
因此,他們向論文一作Dongrui Wang提出挑戰,希望其生成一種包含氯毒素并識別腦癌細胞的CAR。Wang成功了,他的發現促成了該論文的成功發表。
實驗的第一步,Brown及其同事從15個膠質母細胞瘤患者的23個腫瘤樣本中篩選了一組細胞中的氯毒素肽。綠藻毒素緊密附著在幾乎所有患者的腫瘤上,超過80%的細胞結合綠藻毒素。15位患者中只有2位的樣本顯示結合少于總細胞的40%。同樣,在檢查患者來源的膠質母細胞瘤細胞系中的氯毒素結合時,研究小組發現22種培養的細胞系中有21種顯示出超過70%的結合。
相反,目前正在評估CAR-T細胞療法的其他三種靶向劑與腫瘤樣品和培養細胞系的細胞結合較不廣泛且不均勻。
然后,他們使用了Wang的氯毒素CAR,并證明T細胞可以表達CAR并識別已知與氯毒素結合的惡性膠質母細胞瘤細胞。
為了在體內測試CAR,研究人員將患者來源的膠質母細胞瘤細胞植入免疫受損小鼠的大腦中,發現CAR-T細胞與另一種靶向IL13Rα2受體的CAR相比具有強大的抗腫瘤活性,并且是潛在治療膠質母細胞瘤的候選藥物。
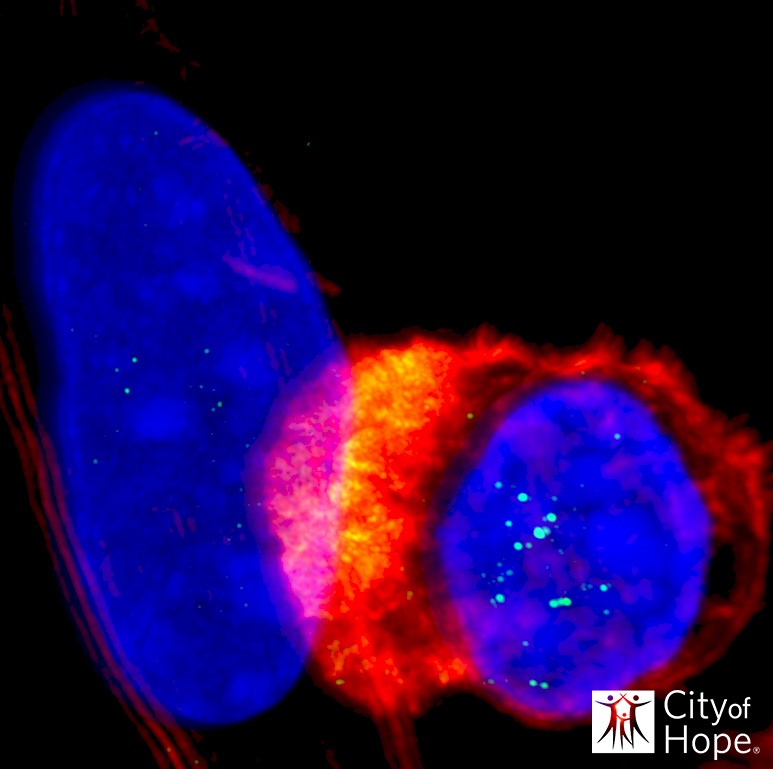
圖丨在左側的惡性膠質母細胞瘤細胞大核(藍色)與右側的CAR-T細胞的小核(藍色)之間的界面處形成了免疫突觸(黃色)。突觸表明T細胞活化,這導致腫瘤殺死。
CAR-T細胞療法的危險之一是脫靶效應,這是因為CAR通過殺死錯誤的細胞而引起不良反應。為了在臨床前模型中評估新型CAR的安全性,研究人員測量了一組非腫瘤人類細胞中的結合,發現很少甚至無法檢測到脫靶識別。換句話說,T細胞幾乎完全攻擊腦癌細胞并幸免于正常細胞。
就連小鼠模型也呼應了這一發現:CAR-T細胞僅靶向膠質母細胞瘤細胞,并且在遞送治療性細胞后,小鼠中沒有不良反應。
Wang說:“我認為鼠模型是非常好的替代品,因為氯毒素受體在人和小鼠之間是保守的。” “因此,我們非常有信心,我們在小鼠中發現的有關該CAR的安全性和功效的信息可以轉化為人類。” Choi指出,但是,在不確切知道靶標如何與癌細胞特異性相互作用的情況下,很難知道對正常人體組織的潛在有害作用。要解決這一問題,實際上取決于第一階段的臨床試驗。”